Appearance
醇(Alcohols)
- 整理者:陈心怡
烷基醇制烷基溴
CBr4-Ph3P是一种非常简单的方法,应用广泛。由于副产品Ph3PO的存在,检查和纯化有时会很混乱。
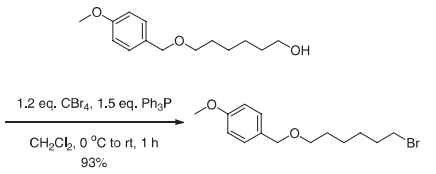
在0℃向存于CH2Cl2中的乙醇(0.800 g, 3.36 mmol)与四氯化碳(1.337 g, 4.03 mmol)的混合物中添加PPh3 (1.319 g, 5.03 mmol)存于CH2Cl2 (3 mL)中的溶液。将反应混合物在室温下搅拌1 h,在减压下浓缩,并通过柱层析纯化,得到溴(0.941 g, 93%产率)。
亦可使用由甲磺酸盐形成,之后用LiBr处理组成的两步序列。这个过程包括两个步骤,但检查和纯化非常简单。在许多情况下,可将溴实施至下一步骤而无需进一步纯化。
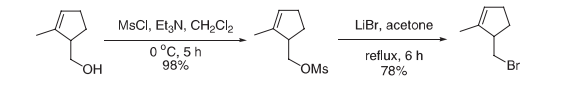
向5-羟甲基-1-甲基环戊烯(3.8 g, 34 mmol)存于CH2Cl2 (50 mL)中于0℃下的溶液中添加三乙胺(5.2 mL, 37 mmol),之后添加甲磺酰氯(2.9 mL, 37 mmol)。在0℃下将混合物搅拌5 h并且然后添加水。分离有机层并用醚萃取水层。经MgSO4干燥合并的有机提取物,并且在减压下去除溶剂,得到6.4 g(98%)(2-甲基环戊-2-烯基)甲基甲磺酸盐,该物质在不进一步纯化的情况下用于下一步。
用溴化锂(8.89 g, 102 mmol)处理含有甲磺酸盐(6.4 g, 34 mmol)存于丙酮(70 mL)中的溶液。将混合物在回流下加热6 h,冷却至室温,用水稀释,用乙醚萃取,合并后的以太提取物经MgSO4干燥。在减压下去除溶剂得到4.6 g(78%) 5-溴甲基-1-甲基环戊烯,该物质被用于下一步而不进一步纯化。
参考文献:Padwa, A.; Dimitroff, M.; Liu, B. Org. Lett. 2000, 2, 3233–3235.2.1.1.2 Alkyl Alcohol to Alkyl Chloride
从烷基醇到烷基氯
CCl4-Ph3P是一种直接且广泛用于将醇转化为烷基氯化物的方法。由于副产品Ph3PO的存在,检测和纯化有时会很棘手。Ph3P的另一种来源是市售的三苯基膦树脂。该树脂的优点是副产物氧化三苯基膦与树脂结合,简化了纯化。
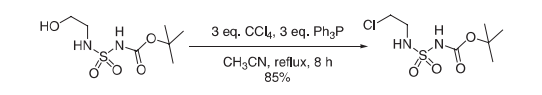
将BOC -磺胺氨基醇(5.35 mmol)、三苯基膦(16.05 mmol)和CCl4 (16.05 mmol)的无水乙腈(100 mL)溶液回流8 h,冷却至室温后真空浓缩。将残余物与二乙醚(3 × 150 mL)研磨。三苯基磷化氢氧化物,沉淀在结合的有机层,被过滤去除。浓缩滤液并在硅胶(CH2Cl2)上纯化残余物,得到产率为85%的N1-BOC,N3-(2-氯乙基)磺胺。
参考文献:Regaïnia, Z.; Abdaoui, M.; Aouf, N.-E.; Dewynter, G.; Montero, J.-L. Tetrahedron 2000, 56, 381–387
一种替代步骤涉及甲磺酸盐形成和氯化锂取代SN2。这种反应应仔细监测(特别是对于活性醇,如烯丙基醇和苄醇),因为氯副产物经常会在原位取代甲磺酸酯。
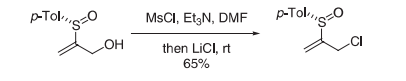
在0℃下用Et3N (630 mg, 6.2 mmol)和甲磺酰氯(705 mg, 6.2 mmol)处理(Ss)-2-(对甲基亚磺酰基)-2-丙烯-1-醇(1.1 g, 5.6 mmol)存于无水二甲基甲酰胺(DMF) (8 mL)中的溶液。使反应混合物升温到室温并且通过薄层色谱(TLC) (CH2Cl2/MeOH 97:3)监测直到检测不到起始醇。接下来用额外的无水DMF (10 mL)稀释混合物,并且逐份添加LiCl (952 mg, 22.4 mmol)。在室温下继续搅拌直至TLC监测显示中间甲磺酸盐的总消耗量。然后将反应混合物蒸发至干燥,将油性残余物吸入乙醚并用盐水洗涤。有机相(无水Na2SO4)干燥和蒸发,得到经快速色谱的粗原料(己烷/EtOAc 85:15),得到烯丙基氯(0.782 g, 65%产率)。
参考文献:Márquez, F.; Llebaria, A.; Delgado, A. Org. Lett. 2000, 2, 547–549.2.1.1.3 Alkyl Alcohol to Alkyl Iodide
烷基醇到烷基碘化
咪唑是一种直接而广泛使用的生成烷基碘化物的方法。由于副产品Ph3PO的存在,检测和纯化有时会很棘手。
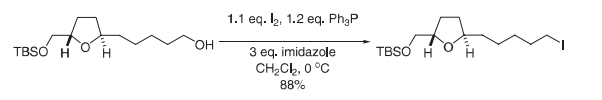
于0℃下将碘(536 mg, 2.11 mmol)添加至咪唑(359 mg, 5.27 mmol)及PPh3 (509 mg, 1.94 mmol)存于CH2Cl2 (10 mL)中之溶液中。将溶液搅拌5 min,然后缓慢添加溶解于CH2Cl2 (2 mL)中的酒精(750 mg, 1.76 mmol)。在不透光的情况下将反应混合物搅拌4 h。然后通过添加Na2S2O3水溶液(10 mL)将其淬火。用甲基第三-丁基醚(MTBE 3 × 20 mL)萃取水层。用饱和NaCl水溶液(10 mL)洗涤合并的有机层并且用MgSO4干燥。在真空中去除溶剂。通过快速柱色谱(20 g二氧化硅,石油醚/MTBE 20:1)纯化粗制产物,生成呈无色油状物形式的碘化物(836 mg, 1.54 mmol, 88%)。
参考文献:Arndt, S.; Emde, U.; Bäurle, S.; Friedriech, T.; Grubert, L.; Koert, U. Chem. Eur. J. 2001, 993–1005.
可通过两步序列(包括甲磺酸盐形成,之后用NaI处理)将烷基醇转化为烷基碘化物。这个过程包括两个步骤,但检查和纯化非常简单。在许多情况下,可将碘化物继续进行至下一步骤而无需进一步纯化。

将乙醇(2.0 g, 12 mmol)逐滴添加至现蒸馏三乙胺(1.82 g, 18 mmol)存于无水CH2Cl2 (35 mL)中于氩下于-10℃之溶液中。搅拌10 min后,添加甲磺酰氯(1.60 g, 14 mmol)。将反应混合物再搅拌20 min且随后用饱和碳酸氢钠水溶液(20 mL)、水(20 mL)及盐水(10 mL)洗涤,干燥并在真空中浓缩。对粗制甲磺酸盐进行色谱,用石油醚:EtOAc(10:1)洗脱,得到呈灰白色蜡状固体的甲磺酸盐(2.68 g, 90%)。向氩下碘化钠(0.525 g, 3.5 mmol)存于热无水丙酮(30 mL)中的溶液中,逐滴添加甲磺酸盐(0.5 g, 2 mmol)存于无水丙酮(25 mL)中的溶液,并在回流下加热所得混合物4 h。然后在真空中去除丙酮,将残留物溶解于醚中。添加水使剩余碘化钠溶解并分离有机层,用水(50 mL)和盐水(50 mL)洗涤,干燥,并在真空中浓缩。
残余物经过层析,用戊烷洗脱,得到淡棕色的碘化物(0.396 g, 71%)。
参考文献:Crombie, B. S.; Smith, C.; Varnavas, C. Z.; Wallace, T. W. J. Chem. Soc. Perkin Trans. 2001, 1, 206–215.
烷基醇到叠氮化物
用二苯基磷酸化叠氮化物处理醇是一步法制造叠氮化物。但用NaN3处理甲磺酸盐也常用于将醇转化为相应叠氮化物(作为两步程序)。
将醇(1.74 g, 4.99 mmol)溶解于甲苯(30 mL)中并冷却至0℃。其次是1,8-二氮杂二环[5.4.0]十一-7-烯(0.91 g, 5.98 mmol)。在0℃下将反应混合物搅拌2 h。随后将溶液加热到25℃,之后添加EtOAc (100 mL)。依次用H2O (1 × 30 mL)、饱和NaHCO3 (1 × 50 mL)和盐水(1 × 50 mL)洗涤有机层。然后经MgSO4干燥有机层,过滤并在真空中浓缩。在硅胶(7.5% EtOAc/己烷)上的色谱提供呈淡黄色油状物形式的叠氮化物(1.58 g, 85%)。
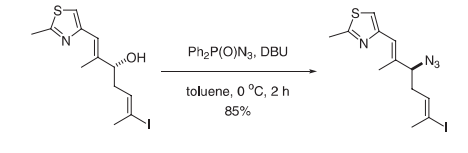
参考文献:Stachel, S. J.; Lee, C. B.; Spassova, M.; Chappell, M. D.; Bornmann, W. G.; Danishefsky, S. J.; Chou, T.-C.; Guan, Y. J. Org. Chem. 2001, 66, 4369–4378.
烷基醇(卤醇)制环氧化物
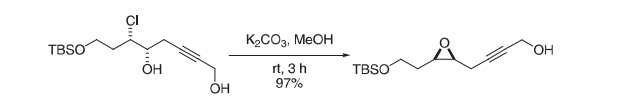
在室温下将存于MeOH (88 mL)中的氯醇(17.61 g, 53.8 mmol)和K2CO3 (13.2 g, 88.5 mmol)搅拌3 h。用乙醚(350 mL)稀释反应混合物,用水(3 × 80 mL)和盐水(100 mL)洗涤,经Na2SO4干燥,并在真空中浓缩。通过快速色谱(SiO2, 20% EtOAc存于己烷中)纯化粗制产物,生成呈无色油状之环氧化物(14.13 g, 97%)。
参考文献:Gao, L.-X.; Murai, A. Heterocycles 1995, 42, 745–774.
醇经伯吉斯脱水剂制烯烃
伯吉斯脱水剂在仲、叔醇生成烯烃中具有较高的效率。它对伯醇不起作用。
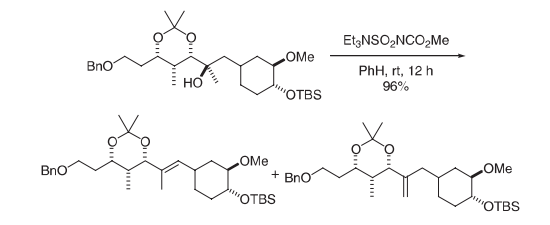
将伯吉斯试剂(62.0 mg, 0.260 mmol)添加到置于1.2 mL苯中的醇(19.6 mg, 0.0336 mmol)溶液中。将异相混合物在氮气中在环境温度下搅拌12 h并且然后短暂加热到50℃以完成消除。冷却后,用5 mL醚将混合物稀释,加入0.5 mL H2O。通过通过硫酸镁塞去除有机层并干燥。快速色谱法(己烷中25%醚)提供的烯烃产物(18.2 mg, 96%)为不可分割的3:1异构体混合物,有利于所期望的三取代烯烃。
参考文献:Nakatsuka, M.; Ragan, J. A.; Sammakia, T.; Smith, D. B.; Uehling, D. E.; Schreiber, S. L. J. Am. Chem. Soc. 1990, 112, 5583–5601.
酒精经马丁硫烷制烯烃
马丁硫烷使仲醇和叔醇脱水生成烯烃,但与伯醇形成醚。
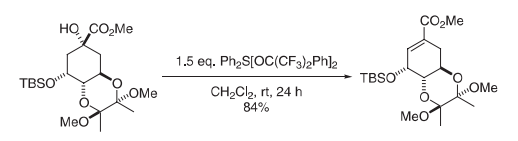
在氮气氛下于室温下将马丁硫烷(0.949 g, 1.41 mmol)存于CH2Cl2 (5 mL)中之溶液缓慢添加至经搅拌之醇(0.41 g, 0.94 mmol)存于CH2Cl2 (10 mL)中之溶液中。将所得淡黄色溶液搅拌24 h,此时在真空中去除溶剂,得到呈淡黄色油状物形式的粗制产物。快速柱层析纯化[SiO2;EtOAc:石油醚(40:60)]之后再结晶(CH3OH/H2O)得到呈无色固体形式的烯烃产物(0.33 g, 84%产率)。
参考文献:Begum, L.; Box, J. M.; Drew, M. G. B.; Harwood, L. M.; Humphreys, J. L.; Lowes, D. J.; Morris, G. A.; Redon, P. M.; Walker, F. M.; Whitehead, R. C. Tetrahedron 2003, 59, 4827–4841.
光延反应(Mitsunobu反应)
古老的光延反应应仍然是手性仲醇立体选择性反转的有力方法。当考虑这个反应时,化学家应该考虑溶剂、膦、偶氮二羧酸和亲核试剂。光延反应最常用的溶剂包括四氢呋喃(THF),二恶烷,CH2Cl2, CHCl3, Et2O, DMF,甲苯和苯。此外,最常用的两种偶氮二羧酸盐是二乙基偶氮唑二羧酸盐(DEAD)和二异丙基二羧酸盐。就磷化氢而言,大多数反应都是在三苯基磷化氢存在的情况下进行的,尽管去除产生的三苯基磷化氢氧化物可能会有问题。此外,羧酸亲核剂在该反应中起关键作用,因此一些羧酸包括甲酸、乙酸、苯甲酸、4-硝基苯甲酸和3,5-二硝基苯甲酸。最后,在某些情况下,将膦与偶氮二羧酸预混并随后添加醇是有利的。虽然光延反应最著名的是手性醇的反转,这一反应的范围已经扩大到包括形成C-N, C-S, c -卤素和C-C键。
Reviews: (a) Hughes, D. L. Org. Prep. Proc. Int. 1996, 28, 127–164. (b) Hughes, D. L. Org. React. 1992, 42, 335–656. (c) Castro, B. R. Org. React. 1983, 29, 1–162. (d) Mitsunobu, O. Synthesis 1981, 1–28.
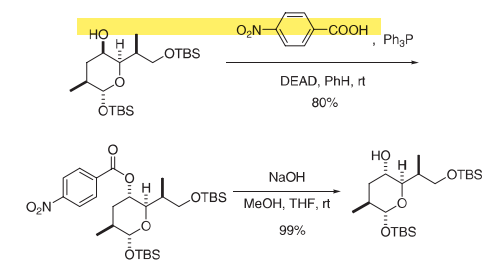
在搅拌的同时将偶氮二羧酸二乙酯(11.6 mL, 74.0 mmol)在室温下逐滴添加到乙醇(6.20 g, 14.9 mmol)、Ph3P (19.7 g, 75.1 mmol)和4-硝基苯甲酸(11.2 g, 67.2 mmol)存于苯(300 mL)中的溶液中,并在室温下将所得橙色溶液搅拌20 h。在减压下浓缩该溶液以得到黏性橙色油状物,将其溶解于最小量CH2Cl2中并通过快速色谱纯化两次;用5%醚/己烷洗脱第一柱,得到部分纯化的酯,将其再次经受色谱,用2%醚/己烷洗脱,得到呈白色结晶固体形式的6.80 g(80%) 4-硝基苯甲酸酯。
将硝基苯甲酸酯(6.80 g, 12.0 mmol)存在于THF/MeOH (10 mL:300 mL)的混合物中,含有粉末状氢氧化钠(1.56 g, 39.0 mmol),在室温下搅拌15 min。在低压下浓缩反应,并将残余物分配于醚/水(100 mL,按体积1:1)中。分离各层,用乙醚(3 × 50 mL)提取水溶液。将组合的有机提取物用盐水洗涤,干燥(MgSO4),过滤,并在减压下浓缩。通过快速色谱纯化粗制残余物,用5%醚/己烷洗脱,提供5.00 g(99%)呈透明油状物的倒置醇。
参考文献:Martin, S. F.; Dodge, J. A.; Burgess, L. E.; Limberakis, C.; Hartmann, M. Tetrahedron 1996, 52, 3229–3246.
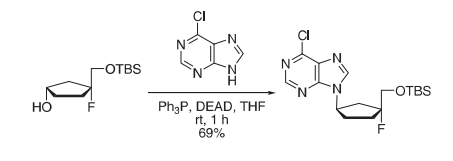
用DEAD(355µL, 2.25 mmol)处理三苯基膦(590 mg, 2.25 mmol)和6-氯嘌呤(348 mg, 2.25 mmol)的无水四氢呋喃(10 mL)悬浮液,室温避光处理1h。然后添加无水THF中的0.56 mmol)并且在室温下将混合物在黑暗中搅拌6 h。蒸发溶剂得到粗产物,通过快速色谱(4:1己烷/EtOAc)纯化所述粗产物,获得呈白色固体形式的149 mg(69%)所述产物。
参考文献:Chong, Y.; Gumina, G.; Chu, C. K. Tetrahedron: Asymmetry 2000, 11, 4853–4875.